TAP Psikofarmakoloji Bülteni - Yeni Ufuklar / Temmuz 2025
Psikiyatri alanında çalışan klinisyenler ve araştırmacılara yönelik hazırlanmıştır.
Bülten Aboneliği
Yeni sayılar yayımlandığında ilk siz haberdar olun! Ücretsiz abonelik için hemen başvurun.
Ücretsiz • İstediğiniz zaman iptal edin
Haberler
Semaglutid ile Lityum Zehirlenmesi!
Klinik pratikte en sık karşılaştığımız sorunlardan biri, hastalarımızın ilaçlara bağlı kilo alımı ve buna bağlı gelişen problemlerdir. Bu problemler, yalnızca fiziksel görünümdeki değişikliklerle sınırlı kalmayıp, ciddi sağlık sorunlarına yol açabilecek riskleri de içermektedir. Farklı ilaçlar ve yöntemlerle kilo alımını kontrol altına almaya çalışsak da bu sorun psikiyatri kliniklerinin görmezden gelemeyeceği kadar yaygındır.
Bu nedenle, yeni obezite tedavileri, özellikle kilolu hastalar ve ilaca bağlı kilo artışı yaşayan bireyler için umut vadetmektedir. Ancak, her ilaçta olduğu gibi, bu yeni tedavilerin de kullanımında fayda-zarar dengesi mutlaka gözetilmelidir.
Son dönemde obezite tedavisinde kullanılmaya başlanan semaglutid, GLP-1 (glukagon benzeri peptid-1) reseptör agonistidir ve mide boşalmasını geciktirerek etki gösterir. Ancak bu ilacın diğer ilaçlarla olası etkileşimleri ve klinik sonuçları henüz tam olarak ortaya konmamıştır. Bu nedenle, sahadan edinilen deneyimlerin paylaşılması, diğer klinisyenler için yol gösterici nitelik taşımaktadır. Yakın zamanda yayımlanan bir vaka sunumunda, yaklaşık iki yıldır stabil lityum düzeyleriyle izlenen ve 14 ay boyunca toksisite belirtisi olmadan günlük 1200 mg oral lityum kullanan bir hastada, semaglutid tedavisinin başlanmasının ardından lityum toksisitesi geliştiği bildirilmiştir.
- Aripiprazol, Brekspiprazol Ve Kariprazin
- İlk Atak Şizofrenide Uzun Süreli Dopamin D2 Blokajı
- Postpartum Depresyonda Nörosteroid Temelli Tedaviler
- Şizofreni Tedavisinde Yeni Nesil Bir Yaklaşım: NBI-117568
- Yeni Bir Molekül: Çocuk ve Ergende Lurasidon
Lityum dozunda herhangi bir değişiklik olmamasına rağmen, serum düzeyi 0,9 mEq/L'den 2,4 mEq/L'ye yükselmiştir. Hidrasyon tedavisi ile düzey normale döndürülmüş ve günlük 600 mg lityum ile etkin plazma düzeyi sağlanabilmiştir. GLP-1 reseptör agonistleri, insülin salınımını artırırken glukagonu baskılayarak ve mide boşalmasını doz bağımlı şekilde geciktirerek etkili olurlar.
Bu gecikmiş gastrik geçiş, eş zamanlı kullanılan oral ilaçların emilim ve dağılımını etkileyebilir. Bu etki özellikle tedavinin ilk dönemlerinde belirgindir ve zamanla gelişen taşifilaksiyle azalabilir. Ayrıca, semaglutid'in iştah baskılayıcı etkileri sıvı, kafein ve tuz alımının azalmasına da yol açabilir; bu da vücutta sıvı dengesini değiştirerek lityum düzeylerinin daha da yükselmesine katkıda bulunabilir. Sonuç olarak, obezite gibi durumların tedavisinde umut vadeden yeni ilaçlar kullanılırken, hastanın mevcut ilaç tedavileriyle olası etkileşimler özellikle göz önünde bulundurulmalıdır.
Dr. Furkan Yazıcı
DOI: 10.1097/JCP.0000000000002017
DOI: 10.1007/5584_2020_496
Yapay Zekâ, Tardiv Diskinezi Taramasında Psikiyatristlerden Daha Hassas
Klinik pratiğimizde antipsikotik ilaçların uzun dönem kullanımına bağlı gelişen önemli komplikasyonlardan biri tardiv diskinezidir (TD). Ancak TD, çoğu zaman gözden kaçmakta ve tanısı gecikmektedir. ABD verilerine göre yaklaşık 2,6 milyon kişiyi etkileyen bu motor bozukluk, yalnızca 40.000 hasta tarafından tedavi edilmektedir. Erken tanı bu tabloyu önlemek adına büyük önem taşımaktadır. TD için onaylanmış tedaviler mevcut olsa da (valbenazin, tetrabenazin), tanıdaki gecikme nedeniyle bu tedavilere erişim sınırlı kalmaktadır.
Yapay zekâ tabanlı bu tür araçların klinik pratiğe girmesiyle, hem hastaların yaşam kalitesinde artış sağlanabileceği hem de sağlık sistemi üzerindeki yükün azaltılabileceği öngörülmektedir.
Son dönemde yayınlanan bir çalışma, video tabanlı yapay zekâ teknolojilerinin bu konuda umut vadettiğini ortaya koymuştur. Üç aşamalı olarak planlanan araştırmada, antipsikotik kullanan hastaların kısa video kayıtları analiz edilmiştir. Yüz, omuz ve el hareketlerini değerlendiren bir algoritma aracılığıyla TD ölçülmüştür.
Çalışmada dikkat çekici sonuçlar elde edildi. Yapay zekâ destekli model, insan gözlemcilerle karşılaştırıldığında daha yüksek duyarlılık ve özgüllük göstermiş; ortalama AUC (area under curve: 1'e yaklaştıkça artan tanıyı ayırt etme gücü) değeri 0,89 olarak bildirilmiştir. Bu değer, modelin TD' yi ayırt etme gücünün oldukça yüksek olduğunu göstermektedir. Araştırmacılar, bu modelin doğrudan tanı yerine geçmese de özellikle telepsikiyatri uygulamalarında tarama aracı olarak kullanılabileceğini ve klinisyenlere zaman kazandırarak riskli hastaların erken belirlenmesine olanak sağlayabileceğini belirtmektedir.
Dr. Gözde Çolak
DOI: 10.4088/JCP.25m15792
Editörden...

Sevgili Meslektaşlarımız, Psikofarmakoloji Derneği'nin 20. yılını kutladığımız bu anlamlı günlerde, sizlere alandaki güncel gelişmeleri ulaştırmayı hedeflediğimiz Psikofarmakolojide Güncel Bültenini tanıtmaktan mutluluk duyuyorum.
Psikiyatrik farmakolojinin 1950'lerde başlayan yolculuğu, özellikle son yıllarda yapay zeka teknolojilerinin katkısıyla hız kazanmış durumda. Artık moleküller bilgisayar ortamında tasarlanabilmekte; önceki hastalardan elde edilen verilerle dayanarak, yeni ilaçların etkinliği ve yan etkileri hakkında öngörüler bulunabilmekteyiz. Bundan sadece 4-5 yıl önce bilim kurgu olarak görülen birçok gelişme, bugün gündelik klinik pratiğimizin bir parçası haline geldi. Bu hızlı değişim, alanımızdaki yenilikleri yakından takip etme sorumluluğunu da beraberinde getiriyor. Bu ihtiyaca yanıt verebilmek adına, Psikofarmakoloji Derneği olarak üç ayda bir ve ilaç endüstrisinden bağımsız olarak yayınlanacak olan bu bülteni hayata geçirdik. Amacımız; yoğun klinik tempoda kısa molalarınızda göz atabileceğiniz, sade, anlaşılır ve güncel içerikler sunmak. Kullandığımız grafiklerin bilgilerin akılda kalıcılığını artıracağına ve içeriğin anlaşılmasını kolaylaştıracağına inanıyoruz.
Türkiye, 1990'lar ve 2000'li yılların başlarında uluslararası ilaç endüstrisinin önemli bir paydaşıydı. Ancak son yıllarda bu tablo değişti. Yeni bir ilacın ruhsat alarak piyasaya girmesi oldukça zaman almakta; hatta eşdeğer ilaçlara erişimde dahi dönemsel sıkıntılar yaşanabilmektedir. Bu durumun ardında çeşitli nedenler ve tartışılan politika tercihleri yer almaktadır. Çok doğaldır ki bu süreçler derneğimizin üyelerinin (önemli bir kısmı doğrudan hasta takibi yapan klinisyenlerden oluşmaktadır) doğrudan etkilemektedir. Bu zorluklarla başa çıkmanın en etkili yolu ise proaktif bir yaklaşım benimsemektir. Bu doğrultuda, bültenimizde tedavi süreçlerindeki zorlukları ve çözüm yollarını ele alan kısa haber ve yorumlara da yer vermeyi planlıyoruz. Klinik deneyimlerinizi bizlerle paylaşmanız, içeriğin daha güçlü ve faydalı hale gelmesini sağlayacaktır.
Bültenimize katkıda bulunmak isteyen tüm meslektaşlarımızın bizimle iletişime geçmesi yeterli olacaktır. Katkılarınız, bu yayını daha zengin ve kapsayıcı hale getirecektir.
Saygılarımla,

Selenyum Nöroprotektif mi?
Son yıllarda nörodejeneratif hastalıklarda tedavi arayışı hızlanmış, birçok ajan özellikle sıçanlar üzerinde test edilmiştir. İnme sonrası nöronal iyileşmenin hızlanması için yapılan bir çalışmada sıçanlarda serebral arterlerde geçici tıkanıklık sonrası selenyum tedavisinin serebral enfarktüs hacmini, oksidatif stresi önemli ölçüde azalttığı ve inme sonrası akut fazda motor performansı arttırdığı gösterilmiştir. Selenyum, kritik antioksidanlardan biri olarak kabul edilen bir eser elementtir.
Çok sayıda araştırma, selenyumun çeşitli nörotoksik ilaçlara karşı nöroprotektif özelliklerini doğrulamıştır. Psikiyatrik bozukluklarda uzun süreli lityum tedavisinin, özellikle sinir sisteminde olmak üzere çoklu organ disfonksiyonu ile komplike hale gelebileceği bilinmektedir. Bunlardan biri de serebellum toksisitesidir ve nadir görülse de ciddi bir yan etkidir. Sıçanlar üzerinde yapılan lityum toksisitesi çalışmasında selenyum uygulamasının oksidatif stres belirteçlerini azalttığı, lityum kaynaklı serebellar değişiklikleri hafiflettiği, Klotho ekspresyonunu artırdığı ve kaspaz-3 ve GFAP (glial fibriler asidik protein) ekspresyonunu düşürdüğü gösterilmiştir. Alzheimer hastalığına yönelik yapılan insan çalışmalarını değerlendiren bir meta-analizde ise selenyum takviyesinin hafif bilişsel bozukluk hastalarında glutatyon peroksidaz (GPX) aktivitesinde ve bazı bilişsel testlerde, Alzheimer hastalarında da mini-mental skorda iyileşme sağladığı gösterildiği bilinmektedir. Sonuç olarak nörodejeneratif doğaya sahip psikiyatrik ve nörolojik hastalıklarda selenyum takviyesi alternatif olarak kullanılabilir.
Dr. Furkan YazıcıDOI: 10.1177/0271678X231156981
DOI: 10.1016/j.tice.2025.102779
DOI: 10.3390/nu14153205
- Prof. Dr. M. Kemal SAYAR
- Prof. Dr. Mesut ÇETİN
- Prof. Dr. Feyza ARICIOĞLU
- Prof. Dr. Ali Saffet Gönül
- Dr. Gözde Çolak
- Yiğit Erdoğan
No:14/15 Kadıköy İstanbul 34738
psychopharmaupdate@gmail.com
Bültenin içeriği ilaç endüstrisinden bağımsızdır.
Aripiprazol, Brekspiprazol Ve Kariprazin
3 Farklı Kız Kardeş
Kariprazinin kısa süre önce Türkiye’deki antipsikotik (AP) piyasasına dahil olması ile beraber parsiyel (kısmi) agonist özellik gösteren AP sayısı üçe çıktı. Her ne kadar aripiprazol (ARI), brekspiprazol (BRX), kariprazin (CAR) ortak bir mekanizmaya sahiplerse de her üçü arasında farmakokinetik, farmakodinamik, kullanım şekilleri, yan etki ve hastalar tarafından tolere edilebilirlikleri açısından farklar bulunmaktadır. Bu farklılıkların daha iyi anlaşılması, klinik uygulamada antipsikotik seçimlerinin daha rasyonel ve bireyselleştirilmiş yaklaşımlarla yapılmasına olanak tanıyacaktır.
Dopamin Reseptör Blokajı ve Klinik Yansımaları
Kapur ve Seeman’ın öncülüğünde yürütülen bir dizi PET çalışması, etkili antipsikotik yanıt için bazal gangliyonlarda dopamin D2 reseptörlerinin yaklaşık %65–75 oranında blokajının yeterli olduğunu göstermiştir. Bu eşik aşıldığında ise prolaktin düzeylerinde artış ve motor yan etkilerin görülme riski belirgin şekilde yükselmektedir. Haklarını vermek kazım ki, bu görüntüleme bulgularından çok daha önce, bazı dikkatli klinisyenler motor yan etkiler ortaya çıkmadan da antipsikotik etkinin sağlanabileceğini, motor yan etkilerin gözlenmesi durumunda ise hastaya gereğinden fazla doz verilmiş olabileceğini öne sürmüşlerdir. Ancak bu iddialarını destekleyecek nitelikte yeterli veri sunulamamıştır. Bu bağlamda, “akıllı ilaçlar” olarak da adlandırılan, kısmi agonist etkiye sahip yeni nesil antipsikotikler ön plana çıkmaktadır. ARI, BRX ve CAR bu grubu temsil eden üç önemli moleküldür.
Aripiprazol (ARI)
ARI, klasik antipsikotiklerden farklı olarak yalnızca dopamin D2 reseptörlerini bloke etmekle kalmaz; aynı zamanda kısmi agonist etkisi sayesinde dopaminerjik aktivitenin belirli ölçüde korunmasına olanak tanır (Eₘₐₓ [dopamin karşısında] ≈ %50–60). Bu özelliği sayesinde dopamin etkisinin yaklaşık %25-30’unun fizyolojik olarak aktif kalması sağlanarak, prolaktin artışı ve parkinsonizm gibi yan etkiler önlenebilmiştir.
Antipsikotiklerin subterapötik dozlarda yeterli klinik etki göstermeyeceği yönündeki kaygı tedavide gereğinden yüksek dozların tercih edilmesine ve istenmeyen yan etkilerin ortaya çıkmasına neden olmaktadır.
Bir mg ARI postsinaptik D2R’lerin yaklaşık %50 sini 10 mg ARI ise yaklaşık %95’ini bloke eder. Klinik gözlemler de bu beklentiyi büyük ölçüde desteklemiş; prolaktin düzeyinde anlamlı artış ve motor yan etkiler nadiren görülmüş, buna karşın akatizi ve huzursuzluk en belirgin yan etkiler olarak öne çıkmıştır. Akatizinin, kısmi agonist etkiden kaynaklanan dopaminerjik uyarıma bağlı geliştiği düşünülmektedir. Akatizi şizofreni hastalarının %8’inde görülürken depresyon hastalarında %25’e kadar çıkabilmektedir. 2002 yılından bu yana FDA onayı ile çeşitli psikiyatrik bozuklukların tedavisinde hem oral hem de uzun etkili enjeksiyon (LAI) formlarıyla yaygın şekilde kullanılmaktadır.
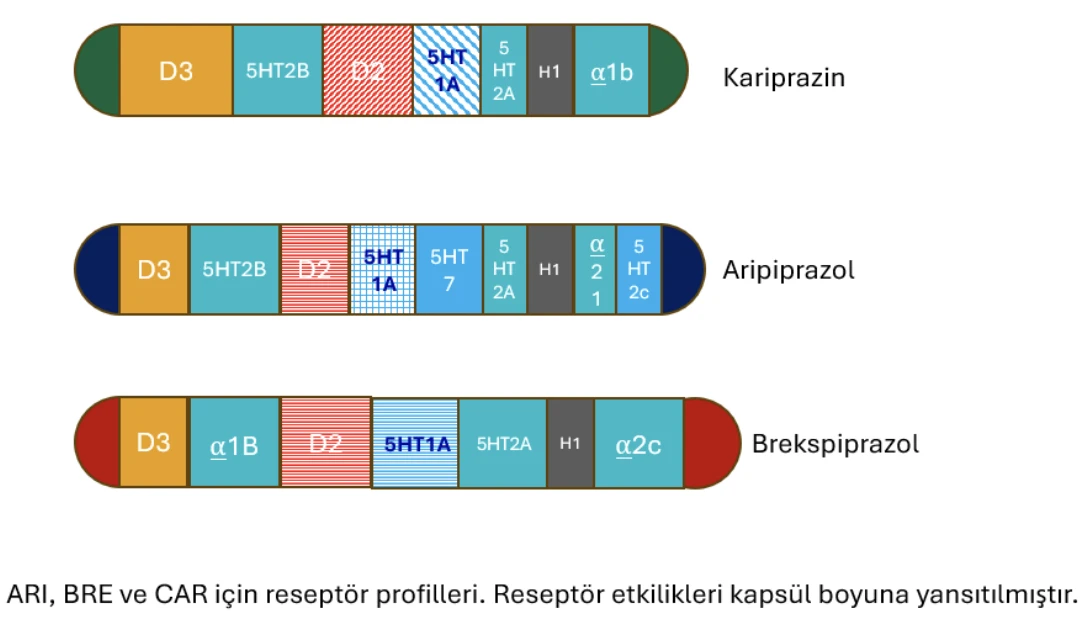
Brekspiprazol (BRX)
BRX, ARI’ye kıyasla daha düşük bir dopamin agonist etkiye sahiptir (Eₘₐₓ ≈ %43); fizyolojik dopamin aktivitesini yaklaşık %20 oranında taklit eder. Bu daha düşük intrinsik aktivite, akatizi gelişme riskini azaltmaktadır. Ayrıca BRX’in 5-HT1A parsiyel agonist, 5-HT2A antagonist ve alfa1B antagonist etkilerinin ARI’ye kıyasla daha belirgin olması, anksiyete ve huzursuzluk gibi yan etkilerin azaltılmasına katkı sağladığı düşünülmektedir. Dört mg BRX postsinaptik reseptörlerin yaklaşık %80 bloke (parsiyel etki nedeni ile intrinsik %20 aktivite dikkate alınmalıdır) etmektedir.
Kariprazin (CAR)
CAR ise, dopamin reseptör profili açısından diğerlerinden ayrılır. D2 reseptörlerine BRX’e benzer şekilde bağlanırken, aynı zamanda yüksek afiniteyle D3 reseptörlerine de bağlanır. D2R için %40 intrinsik aktivite gösterirken D3R için bu oran %60’lara çıkmaktadır. Günlük 3 mg ile D2R’lere %92, D3R’lara %79 oranında bağlanır.
CAR, diğer iki molekülden farklı olarak, şizofrenide primer negatif belirtiler üzerine de etkili olabileceği yönünde bulgulara sahiptir. Bu etkinin, yüksek D3 reseptör afinitesi ile ilişkili olduğu düşünülmektedir. Özellikle ventral tegmental alandaki D3R otoreseptörlerin blokajı ile frontal kortekste dopamin salınımının artması, negatif semptomların düzelmesine katkıda bulunabileceği gibi, bipolar depresyon tedavisinde de terapötik etki sağlayabilir.
Karşılaştırmalı Klinik Etkinlik
Her üç ilacın da parsiyel 5-HT1A agonist, 5-HT2A antagonist ve parsiyel D2 agonist etkileri, majör depresif bozukluk (MDD) tedavisinde antidepresanlara ek tedavi olarak katkı sağladığı düşünülmektedir. Bu bağlamda tahmini NNT (number need to treat) değerleri: ARI için 9, BRX için 12–16, CAR için 9-16 şeklindedir. Kariprazin'in bu etkisine D3R parsiyel ve 5HT1A
full agonist aktivitesinin de katkı sunduğu değerlendirilmektedir. Her üç ilacın da akut şizofreni döneminde etkili olduğu gösterilmiştir. Etkinlik açısından benzer sonuçlar bildirilmiş olup, şizofreni için NNT değerleri şu şekildedir: ARI = 8, BRX= 7, CAR=10. İdame tedavisinde yinelemeyi (relaps) önlemede ise tüm ilaçlar için NNT 4–5 aralığında bildirilmektedir. Farmakokinetik özellikler açısından, bu üç molekül arasında belirgin farklılıklar mevcuttur. Aripiprazol’ün yarı ömrü yaklaşık 75 saattir ve aktif metaboliti dehidro-aripiprazol ile birlikte toplam eliminasyon süresi 86 saate kadar uzamaktadır. Brekspiprazol’ün yarı ömrü ise yaklaşık 94 saat olup, belirgin bir aktif metaboliti bulunmamaktadır. Kariprazin’in yarı ömrü 2–4 gün arasında değişmekte, ancak aktif metabolitlerinin tam eliminasyonu 1–3 haftayı bulabilmektedir. Bu uzun eliminasyon süresi nedeniyle CAR’ın kararlı plazma düzeyine ulaşması zaman almakta, bu durum bazı klinisyenlerin erken dönemde yeterli etki gözlemleyememesi sonucu dozu gereğinden erken artırmasına yol açabilmektedir. Öte yandan, uzun yarı ömür ve aktif metabolit profili sayesinde doz atlamalarında etkide süreklilik sağlanması da CAR’ın avantajlarından biri olarak değerlendirilmektedir.
Her üç ilaç da CYP 2D6 ve CYP 1A2 tarafından metabolize edilirler. Bu enzimleri inhibe eden (fluoksetin, duloksetin, risperidon, paroksetin propranolol) veya artıran (karbamazepin) ilaçlar ana moleküllerin ömrünü uzatıp/kısaltabileceği gibi aktif metabolitlerinin de bedende kalma sürelerini değiştirebilir.
Sonuç ve Klinik Uygulamada Öneriler
Sonuç olarak, ARI,BRX ve CAR; benzer temel etki mekanizmalarına sahip olmalarına rağmen, farmakodinamik profilleri, farmakokinetik özellikleri, klinik endikasyonları ve yan etki tolerabiliteleri açısından belirgin farklılıklar göstermektedir. Bu üç "kız kardeş" molekül, dopamin parsiyel agonistleri olarak şizofreni ve depresyon spektrumundaki birçok olguda etkili tedavi seçenekleri sunmaktadır. Bu ilaçların ayrıntılı biyolojik ve klinik özelliklerinin anlaşılması, tedavi seçimlerinin bireyselleştirilmesi ve yan etki yönetiminin optimize edilmesi açısından büyük önem taşımaktadır.
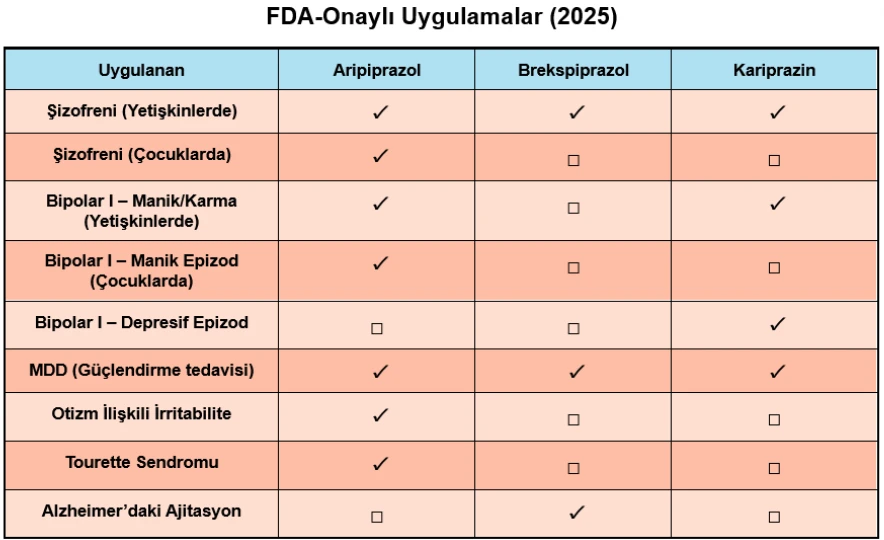
İlk Atak Şizofrenide Uzun Süreli Dopamin D2 Blokajı:
Yeterli mi, Gerekli mi?

Giriş
Şizofreni tedavisinde antipsikotiklerin uzun dönem kullanımı yıllardır önemli bir tartışma konusudur. Bu tartışmalardan biri de, dopamin D2 reseptör blokajının uzun vadede etkinliğini koruyup korumadığıdır. Tiihonen ve arkadaşlarının 2025 yılında American Journal of Psychiatry'de yayımlanan çalışmasında, özellikle ilk atak şizofreni hastaları, sürekli D2 blokajı altında iken , 10 yıla kadar takip edilerek nüks oranları aydınlatılmaya çalışılmıştır.
Çalışma Tasarımı ve Yöntem
Finlandiya'daki ulusal sağlık kayıtları kullanılarak 1996–2014 yılları arasında ilk defa şizofreni tanısı alarak hastaneye yatan 45 yaş altı bireyler taranıp, daha önce antipsikotik kullanımı olmayan 4.788 hasta çalışmaya dahil edilmiştir. 305 kişiye, tanı sonrası ilk 30 gün içinde uzun etkili enjekte edilebilir (LAI) antipsikotik tedavisi başlanmıştır. Bu grup, 'sürekli tedavi' grubunu oluşturmuş, geri kalan hastalar ise tedavisiz, aralıklı ya da ağızdan ilaç kullanan 'diğer' grup olarak tanımlanmıştır. Primer sonlanım noktası, psikotik relaps nedeniyle hastaneye yatış olarak belirlenmiş ve takip süresi 10 yıl olarak tasarlanmıştır..
Bu çalışma, şizofreni tedavisinde sürekli D2 blokajının etkili ve güvenli olduğunu güçlü biçimde ortaya koymaktadır. Özellikle LAI kullanan hastalarda nüks oranlarının düştüğünü göstermektedir.
Sonuçlar – Nüks Oranları ve Değişim
305 kişilik LAI grubunda 10 yıllık takipte %45 oranında nüks gözlenmiştir ve bu da %55’lik bir relapssızlık anlamına gelmektedir. Yıl içinde kişi-yıl başına relaps oranı %26 , beşinci yılda %5’e kadar düşmüştür. Altıncı yıldan itibaren, sadece 4 nüks vakası saptanmış — bu da yılda %3’lük bir orana karşılık gelmektedir. Relaps oranları, tedaviye devam ettikçe belirgin biçimde azalmıştır. Buna karşın, diğer (düzensiz) tedavi grubunda 10 yıl içinde relaps oranı %55 olarak bulunmuştur.
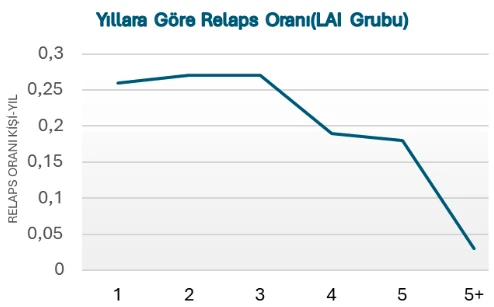
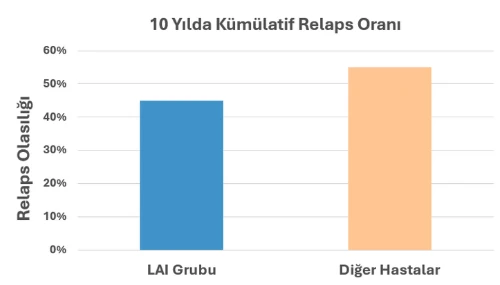
Dopamin Hipersensitivitesi Teorisine Yanıt
Dopamin hipersensitivitesi, uzun süreli D2 blokajının dopamin reseptörlerini daha duyarlı hale getirdiği ve zamanla tedaviye dirençli psikotik ataklara neden olduğu yönünde bir teoridir.
Bu çalışmada ise tam aksi bir durum gözlemlenmiştir: Tedavi süresi uzadıkça relaps oranları azalmış, doz artışına ihtiyaç duyulmamış, hatta ilaç dozları zamanla azalmıştır. 10 yıllık takipte DDD (defined daily dose, tanımlanmış günlük doz) medyanı 1,20'den 1,04'e düşmüş, ayrıca relaps yaşayanlarla yaşamayanlar arasında antikolinerjik kullanım oranının neredeyse aynı olduğu gösterilmiştir.(yaklaşık %19). Bu da yan etkilerin relapsla ilişkisiz olduğunu göstermektedir.
Klinik Pratiğe Yansıması
1. İlk epizod sonrası mümkün olan en kısa sürede LAI başlanması relaps oranlarını azaltabilmektedir.
2. Dopamin süpersensitivitesi teorisi, uzun dönem verilerle desteklenmemektedir.
3. LAI’ler sayesinde tedaviye uyumun artması, uzun vadeli iyilik haline katkıda bulunabilmektedir.
4.Relapslar, tedaviye yanıtı kalıcı olarak düşürebileceği için önlenmesi hayati önemdedir.
5. Şizofreni heterojen bir hastalık olduğundan, dopamin dışı mekanizmaları da hedefleyen stratejiler geliştirilmelidir.
Sonuç ve Yorum
Bu çalışmada, şizofreni tedavisinde sürekli D2 blokajının etkili ve güvenli olduğunu, özellikle LAI kullanan hastalarda zaman içinde nüks oranlarının düştüğü ve ilaç etkinliğinin azalmadığı gösterilmiştir. Tüm bulgular, dopamin hipersensitivitesi teorisini sorgulatırken; dopamin blokajı relapsların önlenmesi, uzun vadeli fonksiyonellik için hala en önemli hedef olmaya devam etmektedir.
Postpartum Depresyonda Nörosteroid Temelli Tedaviler:
Breksanolon ve Oral Alternatifler

Postpartum depresyon (PPD), doğum sonrası dönemde kadınların yaklaşık %10–15’ini etkileyen, işlevsellik kaybına ve ciddi duygudurum belirtilerine yol açabilen bir klinik tablodur. Geleneksel antidepresanların etkileri çoğunlukla 2–4 haftada ortaya çıkar. Ancak PPD’de, özellikle anne-bebek etkileşimi ve erken müdahale açısından daha hızlı etki gösteren ajanlara ihtiyaç vardır. Bu noktada nörosteroid temelli tedaviler dikkat çekmektedir. GABA-A reseptör modülatörü olan breksanolon ve oral alternatifleri, son yıllarda bu alandaki tedavi paradigmasını değiştirmeye başlamıştır.
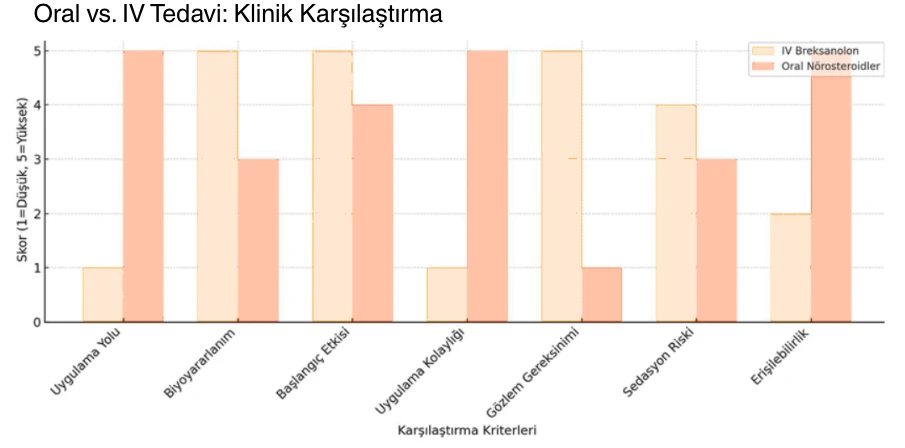
IV Breksanolon: İlk ve Tek Onaylı İntravenöz Tedavi
Breksanolon (Zulresso®️), allopregnanolonun intravenöz formudur. 2019 yılında FDA tarafından PPD tedavisinde kullanılmak üzere onaylanmıştır. GABAA reseptörleri üzerindeki pozitif allosterik etkisi ile hızlı ve güçlü bir etki mekanizması vardır. Faz III çalışmalarda, 60 saatlik infüzyon sonunda 12–24 saat içinde anlamlı bir klinik yanıt elde edilmiştir.
ROBIN ve SKYLARK faz III çalışmaları, zuranolon tedavisinin ilk 3 gün içinde belirgin klinik yanıt sağladığını ve bu etkinin tedavi sonlandıktan sonra da 45 gün boyunca korunduğunu göstermiştir.
Ancak sedasyon, konfüzyon ve nadiren senkop gibi advers etkiler nedeniyle tedavi yalnızca REMS (Risk Değerlendirme ve Azaltma Stratejisi) programına kayıtlı merkezlerde uygulanabilmektedir. Tedavi boyunca hastaneye yatış gereklidir ve annenin bebekle doğrudan ilgilenmesi mümkün değildir.
Zuranolon: Oral Kullanımda Hızlı Etki
Zuranolon 2023 yılında PPD için FDA onayı almış ilk oral nörosteroid ajandır. 14 gün süreyle, günde 1 kez 50 mg dozunda uygulanır. GABA-A reseptörlerini modüle eder. En sık yan etkiler uyku hali, baş dönmesi ve sedasyondur. İlacın etiketinde her dozdan sonra 12 saat boyunca araç ve makine kullanımının önerilmediği belirtilmektedir.
Monoamin Dışı Bir Yol: GABA’yı Hedefleyen Yeni Antidepresanlar
Klasik antidepresanların serotonin üzerinden çalışan yavaş yollarına alternatif olarak, nörosteroidler bambaşka bir kapıyı aralıyor: GABA-A reseptör sistemi. Doğumdan sonra düşen endojen allopregnanolon düzeyleri, GABA-A sisteminde bir “sessizliğe” neden olur. Bu sessizlik, postpartum depresyonun anksiyete, irritabilite ve uykusuzluk gibi ön plandaki semptomlarını açıklamada giderek daha fazla önem kazanıyor. Zuranolon ve breksanolon, GABA-A reseptörlerini pozitif modüle ederek GABA’nın etkisini güçlendirir ve birkaç gün içinde hızlı anksiyolitik ve duygudurum dengeleyici etkiler sağlar; bu mekanizma serotonin veya dopamin sistemine doğrudan etki etmediğinden, ilaç etkileşimleri daha azdır ve etki süresi kısalır.
Yeni Geliştirilen Oral Moleküller: LYT‑300 ve LPCN‑1154
LYT-300: Allopregnanolonun lipit konjugat formudur. Faz I çalışmalar, ağızdan alındığında IV breksanolona benzer plazma düzeylerine ulaşabildiğini göstermiştir. Kortizol stres yanıtında anlamlı azalma saptanmıştır. Faz II çalışmaları planlanmaktadır.
LPCN‑1154: Oral breksanolon formudur. Lipocine firmasının 2024 verilerine göre, IV breksanolon ile biyoeşdeğer farmakokinetik düzey sağlanmıştır. Sedasyon gözlenmemiştir. Kısa, 2 günlük bir tedavi protokolü ile uygulanması hedeflenmektedir.
Şizofreni Tedavisinde Yeni Nesil Bir Yaklaşım:
NBI-1117568

Şizofreninin gelişiminde ve tedavisinde, dopamin (özellikle D2, D3, D4), glutamat (NMDA), asetilkolin (M1 ve M4 muskarinik), serotonin (5-HT2A), nikotinik, TAAR1 (Trace Amine-Associated Receptor 1), Toll-like reseptörler (TLR) ve kannabinoid CB2 gibi çok sayıda reseptör sisteminin rol oynadığı düşünülmektedir. Bu çok katmanlı nörobiyolojik yapı, yalnızca hastalığın belirtilerinin karmaşıklığını değil, aynı zamanda tedavideki zorlukları da beraberinde getirmektedir.
Tipik antipsikotiklerle başlayan ve ardından atipik antipsikotiklerle devam eden klinik yolculuk, şizofreni tedavisinde özellikle pozitif belirtiler üzerinde önemli kazanımlar sağlamıştır. Ancak bu ilaçların getirdiği ekstrapiramidal yan etkiler, kilo alımı, metabolik bozukluklar ve negatif/kognitif semptomlar üzerindeki yetersiz etkileri, araştırmacıların zihninde aynı soruyu yeniden doğurmuştur: “Dopamin D2 reseptörünün ötesinde bir tedavi mümkün mü?”
Bu nedenlerle, son yıllarda yan etki profili daha elverişli alternatif hedefler belirleme çabaları artmış ve kolinerjik sistem, özellikle muskarinik reseptör alt tipleri, dikkat çeken bir araştırma alanı hâline gelmiştir. M1 ve M4 alt tipi muskarinik reseptörlerin, dopaminerjik sistemle etkileşimleri üzerinden şizofreni patofizyolojisinde rol oynayabileceği gösterilmiştir. Bu doğrultuda geliştirilen M1/M4 reseptör agonisti xanomelin, periferik muskarinik yan etkileri azaltmak amacıyla trospium ile kombine edilerek formüle edilmiş ve bu bileşik, 26 Eylül 2024 tarihinde Amerika Birleşik Devletleri Gıda ve İlaç Dairesi (FDA) tarafından şizofreni tedavisinde onay almıştır (1). Sonraki süreçte ise, M1 reseptörüne kıyasla M4 reseptörlerinin daha az periferal yan etkiyle terapötik etki sağlayabileceğine dair bulguların artması, araştırmacıların bu reseptöre yönelmesine neden olmuştur. Preklinik çalışmalar, M4 üzerinden sağlanan bu düzenlemenin pozitif belirtileri baskılayabildiğini, üstelik bunu D2 reseptörünü doğrudan bloke etmeden ve ekstrapiramidal yan etkiler oluşturmadan gerçekleştirebildiğini göstermektedir. M1’e kıyasla daha düşük konvülsiyon riski taşıyan ve periferik etkileri daha sınırlı olan M4 reseptörü, son yıllarda şizofreni tedavisinde umut vadeden bir hedef olarak araştırmacıların artan ilgisini çekmektedir. Merkezi San Diego, California’da bulunan biyofarmasötik şirketi Neurocrine Biosciences, şizofreni tedavisine yönelik geliştirilen M4 selektif agonisti NBI-1117568’in Faz 2 klinik çalışma sonuçlarını 28 Ağustos 2024 tarihinde duyurmuştur (3). 210 katılımcıyla yürütülen bu Faz 2 çalışması, şizofreni tanılı, akut alevlenme veya nüks döneminde olan ve hastaneye yatışı gereken erişkin bireylerde NBI-1117568’in etkinlik, güvenlilik, tolere edilebilirlik ve farmakokinetik özelliklerini değerlendirmeyi amaçlamıştır. Bilgilendirilmiş onamı tamamlayan, çalışmaya başlamadan önce mevcut antipsikotik tedavisini kesmiş olan ve yatılı izlem süresince protokole uyum gösterebilecek durumda olan bireyler çalışmaya dahil edilmiştir. Tıbbi durumu stabil olmayan bireyler, yakın dönemde orta ya da ağır düzeyde madde kullanım bozukluğu öyküsü olanlar, intihar riski taşıyanlar veya araştırmacı tarafından protokole uyumsuzluğu öngörülen bireyler ise dışlanmıştır. Çok merkezli, randomize, çift kör ve plasebo kontrollü olarak tasarlanan çalışma kapsamında farklı doz rejimleri değerlendirilmiştir.
Muskarinik reseptörler, M1’den M5’e kadar beş alt tipe ayrılır. Bu alt tipler arasında M4, özellikle striatumda dopamin salımını fizyolojik olarak düzenleyebilme potansiyeliyle öne çıkar.
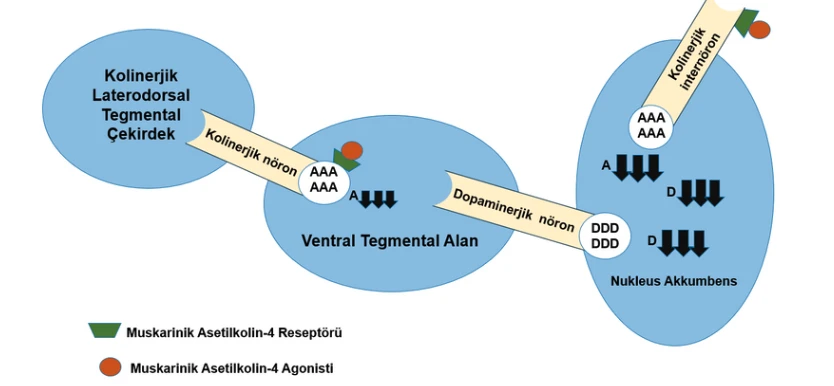
Kolinerjik laterodorsal tegmental çekirdek (LDT)’de bulunun kolinerjik nöronlardan Asetilkolin (A) salgılanır. Muskarinik Asetilkolin 4 agonizması kolinerjik nöron üzerindeki oto-reseptöre bağlanarak reseptörü aktive eder. Reseptör aktivasyonu sonrası asetilkolin salınımı azalır. Böylece ventral tegmantal alandaki asetilkolinle uyarılan dopamin nöronları daha az aktive olur. Bu da nükleus akkumbense olan dopamin salınımında azalma ve psikotik semptomlarda azalma gerçekleştirir. Bir yandan nükleus akkumbenste bulunan kolinerjik ara nöronlarda da muskarinik asetilkolin 4 agonizması aracılığıyla otoreseptör aktivasyonu gerçekleştirilir. Bu durum asetilkolin salınımının azalmasına neden olur. Nükleus akkumbenste asetilkolin düzeyinin azalması bu bölgeye dopamin taşıyan dopaminerjik nöronların aktivitesini azaltır. Bu da nükleus akkumbense olan dopamin salınımında azalma ve psikotik semptomlarda azalma gerçekleştirir.
NBI-1117568'in PANSS Toplam Puanına Etkisi:
Aşağıdaki tablo çalışmada değerlendirilen doz rejimlerine ilişkin PANSS toplam puanı üzerindeki ortalama değişimleri ve istatistiksel anlamlılık düzeylerini özetlemektedir.
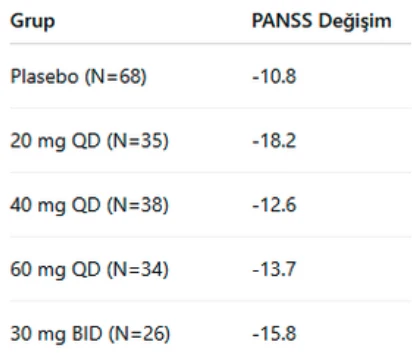
Günde tek doz 20 mg, 40 mg, 60 mg ve günde iki doz 30 mg (toplam 60 mg/gün) NBI-1117568 uygulanan gruplar arasında, en belirgin klinik iyileşme 6. haftada, 20 mg/gün dozunda gözlenmiş; bu grupta PANSS toplam puanında 18,2 puanlık azalma elde edilmiştir. Bu iyileşme, plaseboya kıyasla istatistiksel olarak anlamlı bulunmuştur (p=0,011, etki büyüklüğü: 0,61).
NBI-1117568’in Güvenliği ve Tolerabilitesi
Güvenlik profili açısından, NBI-1117568 tüm doz seviyelerinde genel olarak iyi tolere edilmiştir. Tedaviye bağlı advers olaylar nedeniyle çalışmadan ayrılma oranları, ilacı alan gruplar ile plasebo grubu arasında benzer bulunmuştur. En sık bildirilen yan etkiler arasında uyku hali, baş dönmesi ve baş ağrısı yer almıştır. Gastrointestinal yan etkiler olan bulantı ve kabızlık, düşük sıklıkta görülmüş ve plasebo grubuyla benzer düzeyde seyretmiştir. Ayrıca kardiyovasküler olayların sıklığı düşük olmuş ve klinik açıdan anlamlı bulunmamıştır. Kilo artışı, NBI-1117568 grubunda plaseboya kıyasla artış göstermemiştir. Ek olarak ilaca bağlı ekstrapiramidal semptomlar nadiren bildirilmiştir. Bununla birlikte çalışmada PANSS ölçek puanlarının bildirilmemesi ve 20 mg/gün dozundan daha yüksek dozlarda PANSS toplam puanında istatistiksel olarak anlamlı bir iyileşme gözlenmemesi, dikkat çeken sınırlılıklar arasında yer almaktadır.
Tüm sınırlılıklarına rağmen, NBI-1117568’in yenilikçi etki mekanizması ve umut vadeden erken dönem bulguları, şizofreni tedavisinde yeni bir dönemin habercisi olabileceği yönünde heyecan yaratmaktadır.
Akatizi mi Ajitasyon mu?
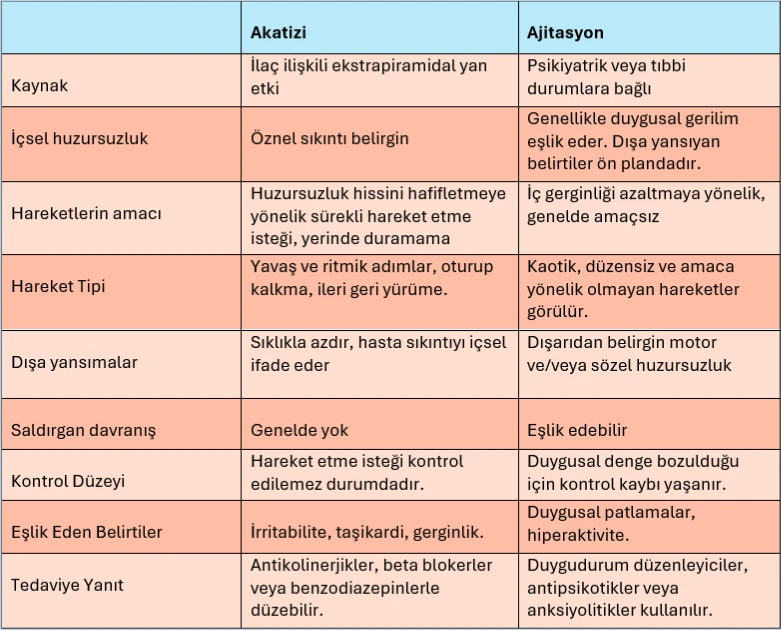
Akatizi ve ajitasyon klinikte sıkça karıştırılan, ancak ayrımı tedavi planını doğrudan etkileyen iki önemli durumdur. Ayırıcı tanıda hastanın şikayetlerini ayrıntılı sorgulamak ve doğrudan gözlem yapmak kritik önem taşır. Bu noktada hareketlerin amacı ve eşlik eden duygusal belirtiler yol göstericidir. Doğru ayrım yapılmadığında yanlış ilaç tedavileri uygulanabilir ve tablo daha da ağırlaşabilir.
Akatizi
Akatizi genellikle ekstrapiramidal yan etki olarak ilaçlara bağlı gelişir ve belirgin içsel huzursuzluk ile karakterizedir. Hasta huzursuzluk hissini azaltmak için sürekli ritmik hareketler (ör. ileri geri yürüme, oturup kalkma) yapar. Dışa yansıma azdır; hasta daha çok içsel sıkıntısını ifade eder ve saldırgan davranış genellikle görülmez. Tanınması önemlidir çünkü bazı çalışmalar akatizinin özellikle erkek hastalarda intihar düşüncesiyle korele olduğunu, ancak ajitasyonla doğrudan ilişkili olmayabileceğini göstermiştir. Akatizi tedavisinde , beta blokerler, benzodiazepinler ve bazı durumlarda antikolinerjikler etkili olabilir.
Ajitasyon
Ajitasyon ise psikiyatrik ya da tıbbi durumlara bağlı gelişir ve emosyonel gerilimle birlikte dışa yansıyan belirgin motor veya sözel huzursuzluk ön plandadır. Hareketler kaotik ve düzensizdir, genelde amaçsızdır. Ajitasyonda saldırgan davranış olabilir. Tedavi yaklaşımı, altta yatan duruma göre duygudurum düzenleyiciler, antipsikotikler veya anksiyolitiklerle yapılır.
Dr. Ayşe Bağcı
Kaynaklar:
DOI:10.1136/bmjopen-2017-017406
DOI:10.1192/j.eurpsy.2021.1287
DOI:10.1097/yco.0b013e32832a16da
DOI:10.3109/15622975.2015.1132007
DOI:10.1017/neu.2022.9
Yeni Bir Molekül:
Çocuk ve Ergende Lurasidon

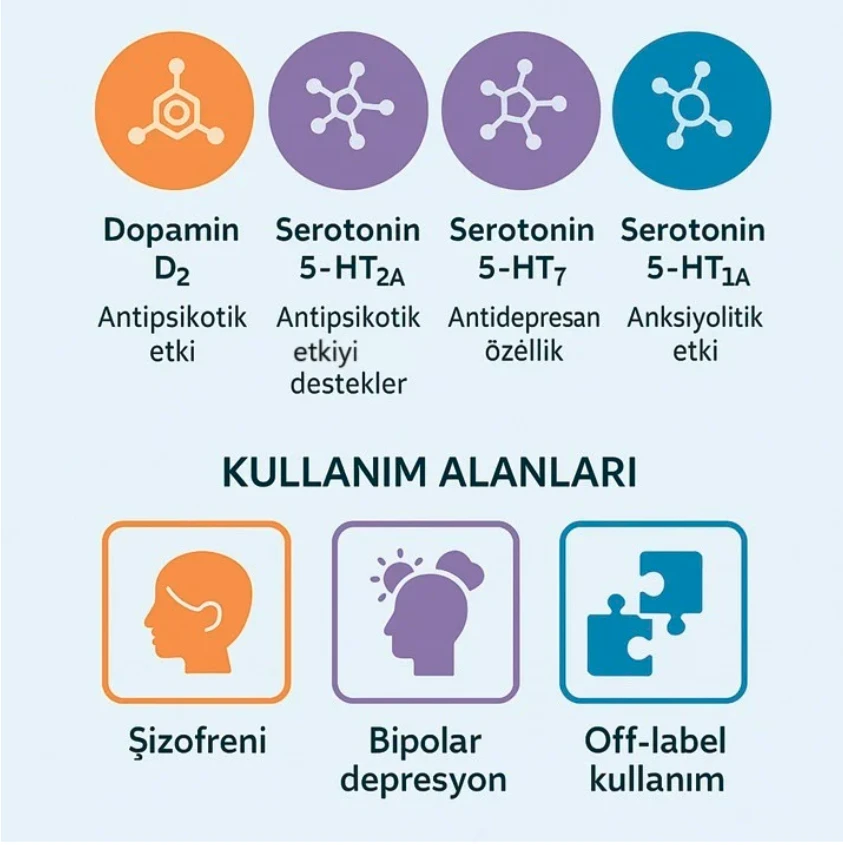
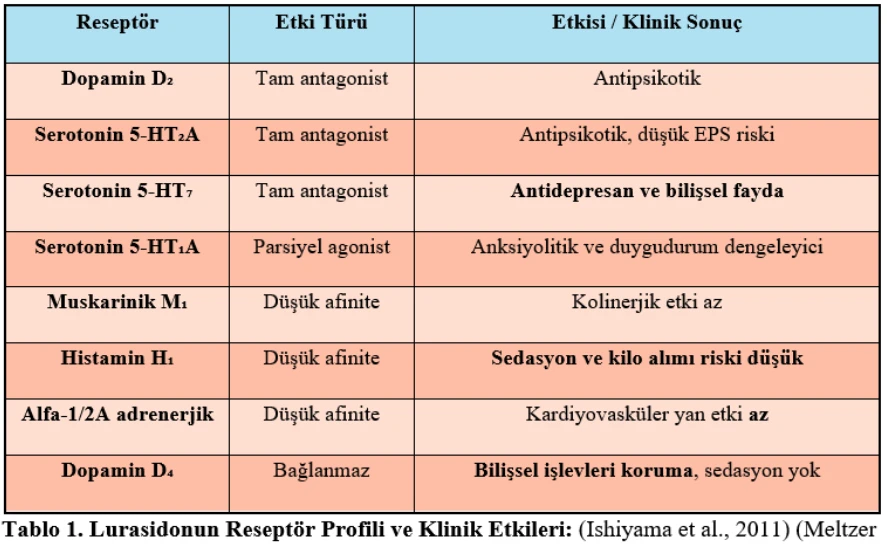
Çocuk psikiyatrisinde onaylı farmakolojik tedavilerin sınırlılığı, karma özellikler gösteren olgularda tedaviyi zorlaştırmakta ve transdiagnostik yaklaşımların önemi artmaktadır. Lurasidon, serotonin ve dopamin sistemleri üzerindeki özgün farmakodinamik özellikleriyle dikkat çeken yeni bir atipik antipsikotiktir. Lurasidon, 13 yaş ve üzeri erken başlangıçlı şizofreni için 2017’de ve 10 yaş üzeri pediatrik bipolar depresyon için 2018’de kullanım için ruhsatlandırılmıştır. IACAPAP kılavuzunda, olanzapin-fluoksetin kombinasyonuyla birlikte pediatrik bipolar depresyonda birinci basamak tedavi olarak önerilmektedir. Lurasidon, benzisotiyazol türevi atipik antipsikotik olup reseptör profili sayesinde antidepresan etki de sunar. Etki mekanizması Tablo 1’de özetlenmiştir.
Farmakokinetik ve Farmakodinamik etkiler:
Lurasidonun CYP3A4 izoenzimi aracılığıyla metabolize olup bu enzimle etkileşime giren güçlü inhibitör ve indükleyicilerle kullanılması kontrendikedir (Azhar & Shaban, 2023). Biyoyararlanımı arttığı için gıda ile birlikte alınması önerilir. Çocuk ve ergenlerde lurasidon genel olarak iyi tolere edilebilmektedir. En sık yan etkiler sedasyon, iştah artışı ve bulantı olup, kilo alımı, QTc uzaması, prolaktin düzeylerinde yükselmedir ve ekstrapiramidal semptomlar gibi ciddi advers etkiler oldukça düşük oranda gözlenmiştir (Findling et al., 2015; Correll et al., 2015). Düşük sedatif etkisi ve bilişsel işlevler üzerinde olumsuz etkilerinin bulunmaması, akademik ve sosyal işlevselliği koruma açısından klinik avantajlar sunmaktadır (DelBello et al., 2017). Lurasidon çocuk ve ergenlerde dozla orantılı, öngörülebilir bir farmakokinetik profile sahiptir. 20–80 mg/gün doz aralığı genel olarak iyi tolere edilirken, 120 mg üzeri dozlarda yan etki riski artmaktadır (Findling et al., 2015).
Etkinlik Bulguları: Erken Başlangıçlı Şizofreni
Erken başlangıçlı şizofreni tedavisinde lurasidon, etkili, güvenli ve metabolik açıdan avantajlı bir antipsikotik olarak öne çıkmaktadır.
Goldman ve arkadaşlarının (2017) yürüttüğü randomize plasebo kontrollü çalışmada, lurasidonun PANSS ve CGI-S skorlarında düzelme sağladığı ve plaseboya göre yüksek tedavi yanıtı gösterdiği bildirilmiştir. Arango ve arkadaşlarının (2020) yaptığı ağ meta-analizinde, lurasidon PANSS ve CGI-S skorlarında plaseboya kıyasla iyileşme sağlamış; olanzapin, risperidon gibi ajanlara göre daha az kilo alımı ile ilişkilendirilmiştir. Correll ve arkadaşlarının (2022) 2 yıllık açık etiketli uzatma çalışmasında, lurasidonla PANSS total skorunda düşüşle %58,3’lük semptom azalımı bildirilmiştir. 2. yıl sonunda remisyon ve iyileşme oranları %50 civarındadır. Yan etki açısından risk düşük bulunmuştur. Bu bulgular, lurasidonun ergen şizofrenisinde uzun dönemli kullanıma uygun ve güvenli bir tedavi seçeneği olduğunu göstermektedir.
Etkinlik Bulguları: Bipolar Bozukluk:
Ergenlerde bipolar depresyon tedavisinde lurasidon, kısa ve uzun vadeli kullanımlarda etkili ve güvenli bir tedavi seçeneği olarak öne çıkmaktadır. DelBello ve arkadaşlarının (2017, 2021) çalışmaları, lurasidonun depresif semptomlarda azalma sağladığını, bu etkinin 2 yıla kadar sürdürülebilir olduğunu ve yan etkilerin genellikle hafif-orta düzeyde seyrettiğini ortaya koymuştur. Klinik yanıt ve remisyon oranlarının yüksekliği, hem işlevsellikte hem de yaşam kalitesinde belirgin artışlarla birlikte gözlenmiştir. Metabolik sendrom açısından riskinin minimal düzeyde olması çocuk yaş grubunda uzun dönemli tedavide avantaj sağlamaktadır. Diao ve arkadaşları (2022), lurasidonun bilişsel işlevler üzerinde ketiapine göre üstünlük sağladığını göstermiştir. Serotonerjik sistem etkileri, BDNF artışı ve antioksidatif yollar aracılığıyla duygudurum ve bilişi iyileştirici etkiler sağlayan lurasidon bütüncül bir fayda sunmaktadır.Depresif ve manik belirti kümeleri arasında geçişe neden olan uykusuzluk ve irritabilite gibi köprü semptomlar, ergenlerde karma belirtilere zemin hazırlayabilmektedir. Singh ve arkadaşlarının aynı örneklemde gerçekleştirdiği çalışmalarda (2020, 2023), köprü semptomlarına sahip olguların lurasidona yanıt verdiği gösterilmiş, subsendromal hipomanik belirtiler eşlik etse de lurasidon her iki belirti kümesinde de iyileşme sağlamıştır. Manik alevlenme riskinin artmadığı ve remisyon oranlarının anlamlı olduğu bildirilmiştir. Her iki analiz aynı randomize çalışmaya dayanmakta olup, sonuçların hipotez üretici düzeyde değerlendirilmesi önemlidir.
Off-label (Endikasyon dışı) Kullanım Alanları
Off-label kullanımlarda, özellikle otizm spektrum bozukluğu (OSB) ve Tourette sendromu gibi durumlarda, irritabilite, saldırganlık ve dürtüsellik gibi belirtilerde lurasidonun olumlu etkiler sağladığını bildiren vaka serileri bulunmaktadır. Ayrıca, antipsikotiklere eklenen lurasidonla ev içi uyum ve sosyal işlevsellikte artış gözlenmiştir (Colizzi et al., 2021; Gupta & Hoover, 2020; Millard & McLaren, 2014). Ancak bu veriler küçük örneklemlere, kombine tedavilere ve plasebo kontrolsüz dizaynlara dayanmaktadır.
Yeni Bir Molekül Olarak Lurasidon Ne Vadediyor?
Lurasidon çocuk ve ergen psikiyatrisinde etkili ve tolere edilebilir bir seçenek olarak ümit vadetmektedir. Ancak dikkat çekilmesi gereken önemli bir nokta, bu yaş grubundaki tanı koyma güçlükleridir. Ergen psikopatolojisi atipik ve dalgalı bir seyir izlemekte ve tanılar arasında geçişkenlik sık görülmektedir. Bu nedenle belirti temelli tedavilerin gerekliliğini artırmaktadır. Ayrıca çocukların kendilerini ifade etmedeki güçlükleri, anamnez güvenilirliğinin düşüklüğü ve damgalanma korkusuyla tanıların ertelenmesi, tedaviye geç başlanmasına neden olabilmektedir.
Sonuç olarak, lurasidon erken başlangıçlı şizofreni ve bipolar depresyon gibi durumlarda semptomatik fayda sağlayabilen, metabolik açıdan avantajlı, bilişsel işlevleri koruyucu özellikleriyle öne çıkan bir antipsikotiktir. Bununla birlikte, çocuk ve ergenlerdeki psikopatolojik heterojenliği dikkate alan daha fazla transdiagnostik ve uzun dönemli çalışmaya gereksinim vardır. Yapılacak kontrollü klinik çalışmalarla, lurasidonun potansiyel endikasyonlarının genişletilmesi ve tanılar arasında ortak semptomlara yönelik kullanımının daha net biçimde tanımlanması beklenmektedir.
Köprü semptomlarına sahip olguların lurasidona yanıt verdiği gösterilmiş, subsendromal hipomanik belirtiler eşlik etse de lurasidon her iki belirti kümesinde de iyileşme sağlamıştır.
- DOI: 10.1007/s00787-019-01425-2
- DOI: 10.1016/j.tice.2025.1473457
- DOI: 10.1016/j.psychres.2020.113609
- DOI: 10.1002/wps.20204
- DOI: 10.1016/j.jaac.2017.10.006
- DOI: 10.1089/cap.2021.0040
- DOI: 10.3390/ph15111403
- DOI: 10.1089/cap.2014.0105
- DOI: 10.1089/cap.2016.0189
- DOI: 10.1089/cap.2019.0069
- DOI: 10.1254/jphs.11082FP
- DOI: 10.1007/s10803-014-2304-3
- DOI: 10.1176/appi.ajp.2011.10060908
- DOI: 10.1089/cap.2013.0116
- DOI: 10.1177/0897190021997011
- DOI: 10.1089/cap.2020.0018
- DOI: 10.2174/1570159X206667112625